Oxi- Ozon
A. Oxi:
I. Vị trí và cấu tạo
- Vị trí của nguyên tố oxi:
+ Z = 8
+ Chu kì 2
+ Nhóm: VIA
- Cấu hình electron nguyên tử:
8O: 1s22s22p4.
- Công thức phân tử và công thức cấu tạo:
+ CTPT: O2.
+ CTCT: O = O.
II. Tính chất vật lí
- Oxi ở trạng thái khí, không màu, không mùi, không vị, nặng hơn không khí:
d O2/K2 = = 1,1
- Oxi tan ít trong nước, dưới áp suất khí quyển hóa lỏng ở -183oC.
III. Tính chất hóa học
- Nguyên tử oxi có 6 electron lớp ngoài cùng.
- Độ âm điện: 3,44 (chỉ nhỏ hơn độ âm điện của flo là 3,98)
Oxi là phi kim hoạt động, dễ nhận thêm 2 electron. Nó thể hiện tính oxi hóa mạnh:
1. Tác dụng với kim loại
– Oxi tác dụng được với hầu hết các kim loại (trừ Ag,Au, Pt):
VD:
2. Tác dụng với phi kim
Oxi tác dụng được với nhiều phi kim (trừ các halogen):
3. Tác dụng với hợp chất
– Oxi tác dụng với nhiều hợp chất vô cơ và hữu cơ:
VD:
Kết luận:
- Oxi có tính oxi hóa mạnh, trong các hợp chất nó có số oxi hóa -2 (trừ hợp chất với flo và trong peoxit).
IV. Ứng dụng
Oxi có rất nhiều ứng dụng như:
- Dùng để luyện gang, thép.
- Dùng trong y học,…(SGK).
V. Điều chế oxi:
1. Điều chế oxi trong phòng thí nghiệm
Trong phòng thí nghiệm, oxi được điều chế bằng cách nhiệt phân các hợp chất giàu oxi và không bền với nhiệt.
VD:
(xúc tác MnO2)
2. Sản xuất oxi trong công nghiệp
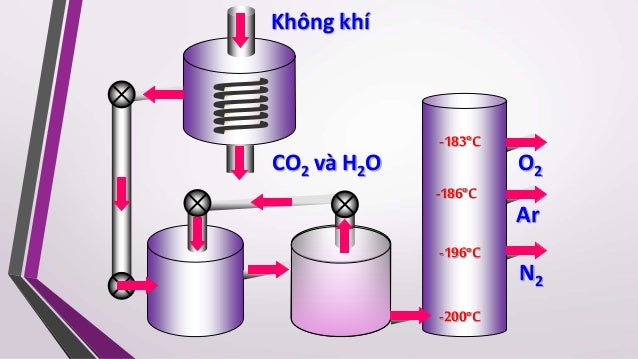
a. Từ không khí:
1. Hóa lỏng Không khí sạch : O2
2. CCPĐ
b. Từ nước: Điện phân nước.
B. Ozon:
I. Tính chất:
+ Tính chất vật lí:
- Ozon ở trạng thái khí, màu xanh nhạt, mùi đặc trưng, hóa lỏng ở -1120C, tan trong nước nhiều hơn oxi khoảng 15 lần.
+ Tính chất hóa học:
- Ozon có tính oxi hóa mạnh và mạnh hơn oxi: Ozon oxi hóa được hầu hết các kim loại (trừ Au, Pt), nhiều phi kim và nhiều hợp chất vô cơ và hữu cơ.
- Ở điều kiện thường, oxi không oxi hóa được bạc, còn ozon oxi hóa được bạc:
II. Ozon trong tự nhiên
- Ozon được tạo ra trong khí quyển khi có sự phóng điện. Trên mặt đất, ozon được tạo do sự oxi hóa một số chất hữu cơ.
- Tầng ozon cách mặt đất 20 - 30 Km. Nó được hình thành do tia tử ngoại của mặt trời chuyển hóa oxi thành ozon:
Tia tử ngoại
III. Ứng dụng
- Tầng ozon bảo vệ con người và sinh vật trên mặt đất khỏi tác hại của các tia tử ngoại.
- Trong công nghiệp dùng để tẩy trắng tinh bột, dầu ăn,…
- Trong y học dùng để chữa sâu răng.
- Trong đời sống dùng để sát trùng nước.










